職位推薦
- 珍格醫療-臨床銷售 15001-20000
- 地奧制藥-醫藥代表 6001-8000
- 普利德醫療-醫療設備銷售經理 面議
- 大唐-兼職招商經理 面議
- 景德中藥-直營經理 6001-8000
- 安邦醫藥-省區招商經理 8001-10000
- 恒瑞醫藥-醫藥信息溝通專員 6001-8000
- 黃河中藥-學術講師 8001-10000
發布日期:2024-12-19 瀏覽次數:58
近日,由中山大學腫瘤防治中心徐瑞華教授、駱卉妍教授、邱妙珍教授團隊開展的一項探索瑞拉芙普-α注射液(SHR-1701)聯合BP102(貝伐珠單抗生物類似藥)和XELOX(奧沙利鉑和卡培他濱)一線治療晚期結直腸癌的研究全文發表于《自然》(Nature)子刊、國際知名醫學期刊《Signal Transduction and Targeted Therapy》(STTT,IF=40.8)。該研究探索了SHR-1701聯合標準一線治療方案是否可以為微衛星穩定型的晚期結直腸癌患者提供更多的治療選擇。結果表明1,62例受試者總體客觀緩解率(ORR)為59.7%(95% CI, 47.3-71.0),中位無進展生存期(PFS)為10.3個月(95% CI, 8.3-13.7),有望為晚期結直腸癌患者提供更多的治療選擇。
研究文章發表于《Signal Transduction and Targeted Therapy》
01研究背景
結直腸癌是世界范圍內最常見的惡性腫瘤之一,中國是結直腸癌高發地區。早期結直腸癌缺乏特異臨床表現,相當一部分患者在初診時已處于局部晚期或出現遠處轉移,喪失手術機會。晚期結直腸癌主要治療包括化療聯合靶向治療。近年來免疫治療在微衛星不穩定/錯配修復基因缺失的結直腸癌中已取得突破性進展,多種免疫治療藥物已獲FDA批準用于該類患者的一線及后線治療2。但微衛星不穩定/錯配修復基因缺失的結直腸癌僅占晚期結直腸癌患者的5%,大部分結直腸癌患者為微衛星穩定型(MSS)3,目前尚未有針對這部分人群的免疫治療藥物獲批。
瑞拉芙普-α注射液(SHR-1701)是恒瑞醫藥自主研發的一種靶向PD-L1和TGF-β的新型雙功能融合蛋白,其用于胃及胃食管結合部腺癌一線治療的上市許可申請已獲國家藥監局受理。臨床前研究表明,SHR-1701與PD-L1、TGF-β1和TGF-β3具有很高的結合親和力,能有效阻斷這兩種通路4。抗血管生成藥物能夠改善血管基質重編程,促進血管正常化和免疫活化,SHR-1701與抗血管生成抑制劑聯合,可逆轉免疫耐受,增敏免疫治療療效5,基于這一理念,徐瑞華教授團隊開展了這項臨床試驗,探索SHR-1701聯合貝伐珠單抗和XELOX化療一線治療晚期結直腸癌的安全性和有效性。
02研究方法
該研究為單臂、多中心的II期階段研究,從2021年6月22日至2022年4月12日,本研究共納入62例晚期一線結直腸癌受試者接受了SHR-1701聯合BP102和XELOX治療,所有受試者均為pMMR(錯配修復功能正常)或MSS,奧沙利鉑最多接受8個周期給藥,SHR-1701聯合治療最長用藥時間為2年。主要研究終點為ORR(研究者評估)和安全性。
03研究結果
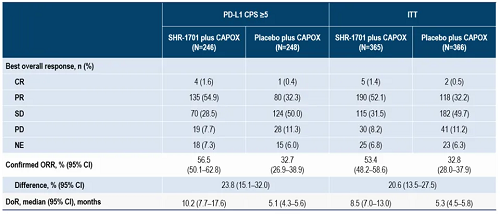
結果表明,62例受試者總體ORR為59.7%(95% CI, 47.3-71.0),包括1例完全緩解(CR)和36例部分緩解(PR),總體疾病控制率(DCR)為83.9% (95% CI, 72.8-91.0)。與基線相比,共有53名受試者(85.5%)的靶病灶面積有所縮小。中位PFS為10.3個月(95% CI,8.3-13.7),OS數據尚未成熟。安全性方面,與既往報道的免疫治療聯合一線化療和貝伐珠單抗治療的研究相近,整體安全性耐受且可控。

圖1:SHR-1701聯合BP102和XELOX一線治療晚期結直腸癌的腫瘤緩解BOR(最佳總體反應)
通過整合DNA測序研究基因組改變與SHR-1701臨床反應之間的關系,發現高腫瘤突變負荷、腫瘤新抗原、SBS15富集與更好的治療應答相關,RAS基因野生型受試者的ORR和PFS更高,基線pSMAD2/3水平越高,臨床療效越好。PD-L1表達陽性的受試者獲得了與PD-L1表達陰性受試者相似的ORR,但PFS更長,表明PD-L1表達可作為反應的部分預測指標,而基線LDH水平升高與較差的預后相關。

圖2:基因組改變與治療療效的相關性
04研究總結
SHR-1701聯合BP102和XELOX化療在一線治療晚期結直腸癌受試者中顯示了初步的療效,總體安全性良好可控,有望為晚期結直腸癌患者提供更多的治療選擇,也為pMMR/MSS結直腸癌的免疫治療提供了更多的循證依據,為有效人群的篩選提供了更多的參考方向。
作為創新型國際化制藥企業,恒瑞醫藥長期堅持“科技為本,為人類創造健康生活”的使命,針對腫瘤等嚴重威脅人類生命健康的疾病持續開展科研攻關,已上市的17款1類創新藥中抗腫瘤創新藥達9款。公司另有90多個自主創新產品正在臨床開發,300余項臨床試驗在國內外開展。
除直腸癌外,SHR-1701目前還在肺癌、胃癌、鼻咽癌等多領域開展臨床研究,未來將有望揭曉更多循證證據,期待SHR-1701為更多腫瘤患者帶來治療新希望。
未來,恒瑞醫藥將繼續堅持“以患者為中心”的理念,重創新,強研發,力爭研制出更多的新藥、好藥,服務“健康中國”,惠及全球患者。
參考文獻:
1.Qiu M, Bai Y, Wang J, et al. Addition of SHR-1701 to first-line capecitabine and oxaliplatin (XELOX) plus bevacizumab for unresectable metastatic colorectal cancer. Sig Transduct Target Ther. 2024; 9: 349. https://doi.org/10.1038/s41392-024-02063-0
2.Overman M J, Lonardi S, Wong K Y M, et al. Durable clinical benefit with nivolumab plus ipilimumab in DNA mismatch repair-deficient/microsatellite instability-high metastatic colorectal cancer. J Clin Oncol. 2018; 36(8): 773-779.
3.Fan A, Wang B, Wang X, et al. Immunotherapy in colorectal cancer: current achievements and future perspective. Int J Biol Sci. 2021; 17(14): 3837-3849.
4.Liu D, Zhou J, Wang Y, et al. Bifunctional anti-PD-L1/TGF-βRII agent SHR-1701 in advanced solid tumors: a dose-escalation, dose-expansion, and clinical-expansion phase 1 trial. BMC Med. 2022; 20(1): 408.
5.Fukumura D, Kloepper J, Amoozgar Z, et al. Enhancing cancer immunotherapy using antiangiogenics: opportunities and challenges. Nat Rev Clin Oncol. 2018; 15(5): 325-340.
300多萬優質簡歷
17年行業積淀
2萬多家合作名企業

微信掃一掃 使用小程序

